PRZEDRUK, oryginał dostępny pod adresem www
Uniwersytet Gdański (www)
Wydział Chemii (www)
Katedry Chemii Bioorganicznej (www)
Kierownik: Prof. dr hab. Krzysztof Rolka
Adres:
ul. Sobieskiego 18/19
80-952 Gdańsk
Kontakt: tel. 58 52 35 386
____________________________________________________________________________
Chromatografia cieczowa na żelu Sephadex, określana też jako sączenie molekularne, jest techniką umożliwiającą analityczny bądź preparatywny rozdział substancji różniących się masą cząsteczkową.
Sephadex jest handlową nazwą złoża stanowiącego poprzecznie usieciowane łańcuchy dekstranu. żel ten ma postać granulek o średnicy 10-300 µm, które w zależności od usieciowenia, różnią się zdolnością wchłaniania wody. Cecha ta decyduje o właściwościach rozdzielczych żelu. Produkowane są złoża, w których stopień usieciowienia określa cyfra znajdująca się przy dużej literze „G” (od G-10 do G-200), przy czym im większa cyfra tym niższe usieciowienie.
Mechanizm sączenia na żelu w największym uproszczeniu przedstawia się następująco. Cząsteczki większe niż pory napęczniałych ziaren żelu nie mogą penetrować do ich wnętrza, a więc przepływają wyłącznie wraz z fazą ruchomą i są eluowane jako pierwsze. Mniejsze cząsteczki wnikające w różnym stopniu do wnętrza granulek żelu, w zależności od swego kształtu i rozmiaru, eluowane są w kolejności zmniejszania się ich masy cząsteczkowej. Charakteryzując w doświadczeniu stosowaną kolumnę chromatograficzną oraz zachowanie się rozdzielanych substancji, stosuje się następujące pojęcia: – objętość całkowita złoża – Vtot;
– objętość pusta kolumny Vo, tzn. objętość eluentu znajdującego się pomiędzy ziarnami żelu;
– objętość rozpuszczalnika związanego z żelem Vi;
– objętość matrycy żelu Vg;
– objętość elucyjna Ve, charakterystyczna dla danej substancji;
Pomiędzy tak zdefiniowanymi wielkościami zachodzi następująca zależność:
Vtot = Vo + Vi + Vg
Rozpatrując sączenie molekularne na żelu jako szczególny przypadek chromatografii podziałowej, zastosować można zależność pomiędzy objętością elucyjną substancji Ve, a współczynnikiem podziału K tej substancji między fazę stacjonarną i ruchomą (charakterystycznym dla tej substancji):
Ve = Vo + KVg
gdzie: K – współczynnik podziału, Vo – faza ruchoma, Vg – faza stacjonarna.
W chromatografii na żelu, w zależności od zdefiniowania fazy stacjonarnej stosuje się dwa różne współczynniki podziału.
– Jeżeli jako fazę stacjonarną traktuje się rozpuszczalnik związany z żelem (Vi), otrzymujemy zależność:
KD = (Ve – Vo) / Vi
– Jeśli jako fazę stacjonarną przyjmujemy całą fazę żelu (tzn. Vi + Vg), otrzymujemy zależność:
KAV = (Ve – Vo) / Vtot
Wartość KAV jest łatwiejsza do wyznaczenia, stąd też częściej jest stosowana w praktyce. Jej wartości w zależności od wielkości cząsteczek leżą w granicach 0-1.
W praktyce sączenie molekularne stosuje się do:
– rozdziału substancji różniących się masą cząsteczkową
– odsalania substancji, których masy cząsteczkowe są znacznie większe od masy cząsteczkowej soli obecnej w próbce
– wyznaczania mas cząsteczkowych związków.
Odczynniki i sprzęt laboratoryjny:
1. Kolumna chromatograficzna o wymiarach 2×30 cm
2. Cylinder miarowy na 50 mL
3. Pipety miarowe
4. Probówki szklane zwykłe
5. Strzykawka na 1 mL z igłą
6. Zlewki na 500 mL
7. Erlenmajerka na 500 mL
8. Spektrofotometr UV-Vis
9. Sephadex G-75, 90 mL zawiesiny w 0,9% NaCl
10. Eluent: 0,9% roztwór NaCl, 500 mL
11. Próbka do rozdziału: 0,5 mL 0,9% roztworu NaCl zawierającego 2% sacharozy oraz: 1 mg Blue Dextranu (M. cz. około 2000000), 5 mg albuminy z osocza bydlęcego (BSA) (M. cz. 68000), 5 mg inhibitora trypsyny wyodrębnionego z nasion soi (STI) (M. cz. około 20000) i 10 mg CoCl2 (M. cz. 130)
12. Wata szklana
13. Kuwety kwarcowe.
Wykonanie doświadczenia:
Przygotowanie kolumny chromatograficznej
Kolumnę chromatograficzną umieścić pionowo w statywie, zamknąć jej wylot zaciskaczem i wlać do niej około 10 mL roztworu NaCl. Następnie przy pomocy bagietki umieścić na dnie kolumny tamponik z waty szklanej uważając, aby nie powstały pęcherzyki powietrza. Ostrożnie wlać (po bagietce) do kolumny zamieszaną uprzednio zawiesinę żelu (przed jej zamieszaniem zawiesina w zlewce powinna być przygotowana tak, aby 2/3 jej objętości stanowił żel, a 1/3 roztwór NaCl). Odczekać, aż na dnie kolumny uformuje się warstwa żelu 3-5 cm, po czym ostrożnie otworzyć zacisk kolumny. Roztwór powinien wypływać z szybkością 1 kropli/sek. Wysokość uformowanego żelu powinna wynosić 20 cm. Następnie na szczycie kolumny ostrożnie umieścić krążek z bibuły filtracyjnej i zamknąć wylot kolumny, pozostawiwszy nad powierzchnią co najmniej 2 cm roztworu.
Uwaga: uformowana kolumna musi być zawsze przykryta warstwą roztworu.
Równoważenie kolumny chromatograficznej
Kolumnę z uformowanym żelem Sephadex G-75 połączyć ze zbiornikiem zawierającym 300 mL eluentu, otworzyć zacisk u dołu kolumny i przepuścić przez nią ok. 80 mL roztworu. Szybkość przepływu powinna wynosić ok. 1 mL/min. Szybkość tę reguluje się poprzez zmianę położenia zbiornika w stosunku do kolumny.
Rozdział na kolumnie chromatograficznej
Po przemyciu kolumny zaznaczyć dolną i górną granicę złoża, przerwać dopływ cieczy do kolumny pozostawiając nad powierzchnią żelu minimalną warstwę roztworu. Przy pomocy strzykawki nanieść ostrożnie (nie naruszając złoża) na czoło kolumny 0,5 mL roztworu badanej próbki (uwaga: próbkę należy przefiltrować przed naniesieniem na kolumnę). Otworzyć ostrożnie wylot kolumny, umieszczając jako odbieralnik wycieku cylinder miarowy. Po wsiąknięciu próbki w żel należy zamknąć wylot kolumny, a następnie przy użyciu wypłukanej uprzednio strzykawki wprowadzić tyle roztworu eluentu, aby jego warstwa nad powierzchnią żelu wynosiła ok. 2 cm. Do kolumny podłączyć rezerwuar z eluentem i otworzyć jej wylot. Pierwsze 10 mL wycieku zbierać do cylindra miarowego, a następnie zbierać frakcje o objętości 2,5 mL do probówek aż do momentu całkowitego wyeluowania chlorku kobaltu (II). Przerwać elucję, wylać żel z kolumny do zlewki. Zmierzyć objętość, jaką zajmował żel, napełniając kolumnę wodą i mierząc cylindrem objętość wody mieszczącej się w części kolumny zaznaczonej uprzednio kreskami. Wartość tę (Vtot) zanotować.
Wyniki i obliczenia
Zmierzyć absorbcję frakcji zawierających: Blue Dextran przy 620 nm, albuminy z osocza bydlęcego (BSA) przy 280 nm, mioglobiny i CoCl2 przy 510 nm. Zanotować wyniki:
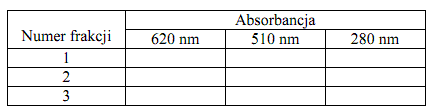
Sporządzić na papierze milimetrowym lub posługując się odpowiednim programem komputerowym diagram elucji. Obliczyć dla rozdzielanych związków wartości KAV w/g wzoru:
KAV = (Ve – Vo) / (Vtot – Vo)
gdzie: Ve – objętość elucyjna badanej substancji, Vo – objętość elucyjna Blue Dextranu, Vtot -objętość całkowita złoża.
Wyniki umieścić w tablicy:


