Na podstawie elektroforezy białek
Elektroforezę możemy zdefiniować jako wędrówkę jonów w polu elektrycznym. Prąd elektryczny w przewodnikach metalowych powstaje z powodu ruchu elektronów, w roztworach natomiast poruszają się jony. Elektroda o znaku ujemnym, czyli katoda, oddaje elektrony, natomiast anoda elektrony pobiera. Jony, które zostały „obdarowane” elektronami przez katodę, są naładowane ujemnie i migrują do anody. Z tego tez powodu ujemnie naładowane jony nazywamy anionami. Jony, które utraciły elektrony poprzez kontakt z anodą, poruszają się w kierunku katody i nazywamy je kationami. Różnica potencjałów pomiędzy anodą i katodą nazywana jest napięciem. Jeżeli roztwór między katodą i anodą ma stały skład oraz stały opór to napięcie ma charakter linearny i podawane jest w voltach na cm-1. Białka poruszające się w żelu elektroforetycznym podlegają siłom tarcia, które zależą w znacznej mierze od szybkości ich ruchu. Bardzo szybko osiągają one prędkość przy której siła je napędzająca równa się sile tarcia. Szybkość poruszania się cząstek w żelu do elektroforezy, w znaczącej mierze zależy od ich ładunku oraz od budowy ośrodka, w którym się poruszają. W elektroforezie wykorzystuje się zasadę w myśl której cząsteczki poruszają się z różnymi prędkościami i na tej podstawie zachodzi ich rozdział. Ponieważ przyłożony ładunek oraz siły tarcia powodują generowanie ciepła musimy stale kontrolować warunki w jakich zachodzi elektroforeza.
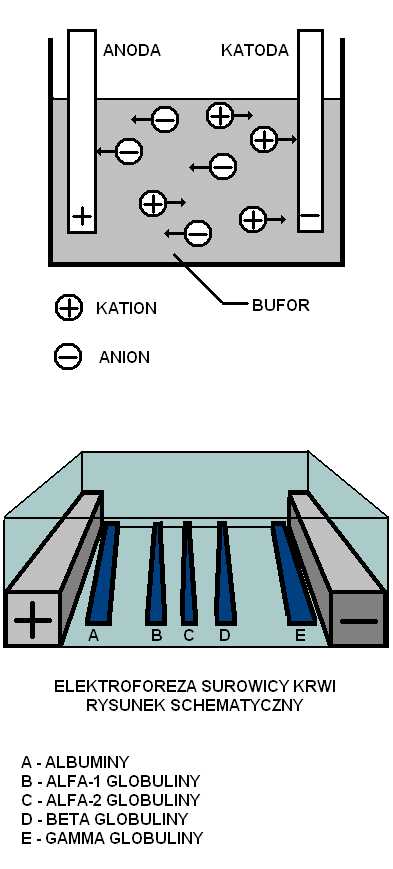
Również bufor, który stosujemy do elektroforezy ma na nią duży wpływ. Po pierwsze, pH buforu ma wpływ na ładunek białka, kierunek oraz szybkość jego migracji. Po drugie, siła jonowa buforu ma bezpośrednie przełożenie na szybkość migracji białek.
Niska siła jonowa buforu powoduje szybszą migrację rozdzielanych białek, a wysoka wolniejszą. Niska siła jonowa przyczynia się do redukcji produkcji ciepła. Ważna jest również mobilność jonów znajdujących się w buforze. Zależy ona w znacznej mierze od tego jakiej wielkości są molekuły jonów. Większe poruszają się wolniej i generują mniej ciepła.

