Nested PCR – nazywany również gniazdowym PCR, zagnieżdżonym PCR lub wewnętrznym PCR – jest to metoda zaprojektowana w celu zwiększania wrażliwości standardowej techniki łańcuchowej reakcji polimerazy. Jej produkt może być wykorzystywany jako sonda molekularna w hybrydyzacji lub kontrola specyficzności namnażania matrycy. Wymaga ona jednak o wiele większej wiedzy na temat powielanego fragmentu niż standardowy PCR.
Polega ona na wykonaniu dwuetapowej amplifikacji. Produkty powstające w pierwszym etapie mogą wciąż zawierać niespecyficznie namnożone fragmenty DNA. Niepożądane tło zostaje zredukowane dzięki przeprowadzeniu kolejnej reakcji. Produkt amplifikacji uzyskany w pierwszym PCR stanowi matrycę powielaną w drugim PCR, co znacznie zwiększa wrażliwość metody i jednocześnie nie obniża jej specyficzności.
W drugim etapie wykorzystuje się specjalnie zaprojektowane pary starterów, które muszą być zlokalizowane wewnątrz powielonego fragmentu DNA. Nazywa się je primerami wewnętrznymi lub inaczej primerami nested. (ang. forward inner primer FI i rewers inner primer RI). Pierwsze pary starterów określana jest natomiast mianem primerów zewnętrznych (ang. forward outer primer FO i rewers outer primer RO).
W przypadku, gdy niemożliwe jest zastosowanie dwóch różnych par starterów i wykonanie całego nested PCR, specyficzność i wrażliwość reakcji można sprawdzić poprzez przeprowadzenie tzw. semi-nested PCR. Metoda ta polega na użyciu jednego primera wewnętrznego, współdziałającego ze starterem charakterystycznym dla pierwszego etapu.
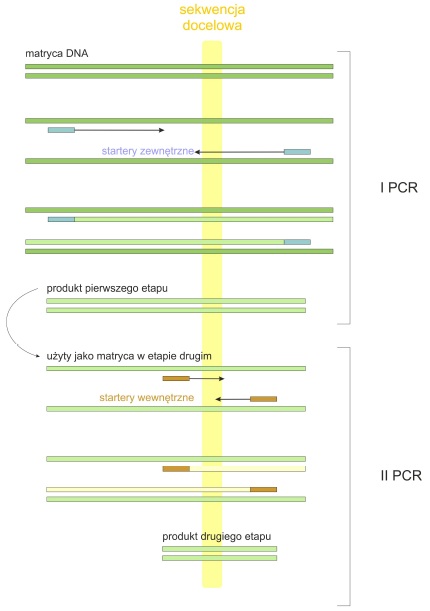
Rys. 1. Zasada metody nested PCR
Wewnętrzny PCR pozwala na przeprowadzenie większej liczby cykli i uzyskanie dużej ilości produktu. Warunkiem jest uzupełnione komponentów reakcji, np. polimerazy Taq. Planując nested PCR należy uwzględnić dodatkowe koszta związane ze zwiększonym zużyciem odczynników oraz zaprojektowaniem i syntezą dodatkowej pary primerów. Najczęstszym problemem tej metody jest jednak podatność na zanieczyszczenia badanego materiału. Próbówki reakcyjne z pierwszego etapu muszą zostać otwarte, aby w ten sposób umożliwić przeniesienie uzyskanego produktu do nowej próbówki i poddanie go kolejnej reakcji.
Aby zminimalizować ryzyko wystąpienia zanieczyszczeń, można przeprowadzić obie reakcje w jednej próbówce. Wszystkie startery dodaje się wówczas równocześnie do przygotowywanej mieszaniny reakcyjnej. Jest to zatem jednoetapowa amplifikacja z użyciem dwóch różnych par primerów. W metodzie tej, wewnętrzne startery są tak zaprojektowane, aby mieć niższą temperaturę topnienia (ang. melting temperature – Tm), np. 45°C, w porównaniu z zewnętrznymi (np. 80°C).
Podczas pierwszej tury PCR, temperatura elongacji musi być odpowiednio dobrana i umożliwiać hybrydyzację tylko zewnętrznej parze, a zatem prowadzić do powstawania długich fragmentów DNA. Etap ten trwa przez 15 do 20 cykli i jest przeprowadzany w następujących warunkach: denaturacja 95°C przez 20 sekund, dołączenie primerów i elongacja 72°C przez 30 sekund.
Kolejne 16 cykli wykonuje się następująco: denaturacja w 92°C – 20 sekund, dołączenie primerów – 20 sekund, rozpoczynając od temperatury 66°C i redukując ją o 2°C co dwa kolejne cykle, elongacja w 72°C – 20 sekund. W tym etapie zachodzi jeszcze resztkowa amplifikacja zewnętrznych primerów i tworzą się produkty różnej wielkości, powstające między innymi w wyniku współdziałania primerów zewnętrznych i wewnętrznych.
Podczas trzeciego etapu temperatura zostaje obniżana na tyle, aby umożliwić funkcjonowanie starterów nested i syntezę krótkich fragmentów. Faza ta obejmuje 37-45 cykli (denaturacja 88°C – 20 sekund, dołączenie primerów 50°C- 20 sekund, elongacja 72°C – 20 sekund).
Pomimo swoich zalet metoda z wykorzystaniem jednej próbówki, nie jest tak samo skuteczna jak oryginalny zagnieżdżony PCR.
Podczas projektowania starterów do nested PCR obowiązują takie same zasady jak przy standardowej łańcuchowej reakcji polimerazy. Trzeba jednak dodatkowo uwzględnić możliwość parowania się primerów i tworzenia zakłócających wynik dimerów (ang. primer-dimer). Jeżeli startery są równocześnie dodawane do mieszaniny reakcyjnej, wtedy należy je zaprojektować w taki sposób, by temperatura topnienia primerów nested była niższa niż primerów zewnętrznych. Różnica ta musi być na tyle duża, żeby zabezpieczyć startery wewnętrzne przed hybrydyzacją podczas początkowych cykli. Najprostszą metodą na uzyskanie tego efektu jest skrócenie długości starterów nested w porównaniu z tymi wykorzystywanymi w pierwszym etapie (np. 18-20 zasad / 25-28 zasad). Powinny one również maksymalnie różnić się od siebie zawartością guaniny i cytozyny. Ilość użytych starterów nested powinna znacznie przewyższać (około 40) liczbę primerów zewnętrznych. Dodatkowe zastosowanie krótszego czasu hybrydyzacji i elongacji w drugim etapie PCR faworyzuje primery wewnętrzne i powoduje produkcję krótszych fragmentów.
Zobacz również:
PCR
RT-PCR
Real-time PCR
Multipleks PCR
MLPA PCR
Autor: Anna Kurcek
Literatura:
• Carl W. Dieffenbach, Gabriela S. Dveksler „PCR Primer: A Laboratory Manual” Second Edition; Cold Spring Harbor Laboratory Press, New York 2003;
• Anna Raszka, Aleksandra Ziembińska, Anna Wiechetek “Metody I techniki biologii molekularnej w biotechnologii środowiskowej”; Środowisko Czasopismo Techniczne Politechniki Krakowskiej 2-Ś, zeszyt 2, rok 106 (2009);
• http://www.slidefinder.net „Najważniejsze odmiany techniki PCR”;

