Metoda mikromacierzy DNA polega na hybrydyzacji badanego materiału z DNA związanym z nośnikiem, którą opisał i opracował ilościowo Edwin Southern. Podstawy do opracowania mikromacierzy DNA dała powszechnie stosowana do końca lat 70. metoda dot- i slot-blottingu DNA – metoda immobilizowania dużych ilości DNA w uporządkowanych szeregach do błon nitrocelulozowych lub nylonowych.
Krótka historia
Przełom XX i XXI wieku stał się początkiem nowej ery w dziedzinie badań transkryptomicznych – globalnej analizy ekspresji genów. Pomysł jednoczesnego badania ekspresji dużej liczby genów nie pojawił się jednak nagle. Naukowcy od wielu lat próbowali stworzyć metody badawcze, które pozwoliłyby na jednoczesną analizę ekspresji wielu tysięcy genów, co umożliwiłoby nie tylko masową analizę ich stanu funkcjonalnego, ale również określenie ich wzajemnych relacji.
Naukowcy ze Stanford University (USA) w 1995 roku zaproponowali nowe narzędzie badawcze – mikromacierze DNA (DNA microarray, biochip) w formie jaką znamy dzisiaj – szklanej płytki z nadrukowanymi sekwencjami cDNA. Metoda analizy ekspresji genów przy pomocy mikromacierzy pozwoliła na jednoczesną ocenę aktywności kilku tysięcy genów w kilku powtórzeniach podczas jednej analizy. Dzięki temu możliwe jest przeprowadzenie doświadczenia, do którego, jeszcze kilka lat temu konieczne było zaangażowanie kilkunastu naukowców i czas mierzony w latach. Metoda ta otworzyła drogę do dynamicznego rozwoju genomiki funkcjonalnej (functional genomics).
Co to jest mikromacierz?
Mikromacierze to szklane lub plastikowe płytki wielkości mikroskopowego szkiełka podstawowego, na których w znanej kolejności (w rzędach i kolumnach tworzących submacierze), metodą kontaktową lub piezoelektryczną (podobną do tej stosowanej w drukarkach atramentowych) nanoszone zostają jednoniciowe sondy cDNA (w przypadku macierzy cDNA) lub metodą fotolitografii syntetyzowane są bezpośrednio na płytkach kilkudziesięcionukleotydowe sondy, w przypadku mikromacierzy oligonukleotydowych, tzw. chipów DNA. Sondy na ogół mają średnicę około 100μm i znajdują się od siebie w odległości 200-300μm.
Długość sond cDNA waha się w granicach 500-5000 nukleotydów. Otrzymuje się je przez amplifikację metodą RT-PCR. Przygotowanie sond do umieszczenia na mikromacierzy jest więc stosunkowo proste, wystarczy dobrze zaprojektować startery do selektywnej i wydajnej amplifikacji wybranych części genów, bez konieczności poznania całej sekwencji takiej sondy. Niestety, otrzymanie każdej sondy wymaga przeprowadzenia oddzielnej reakcji. Po amplifikacji i oczyszczeniu, sondy nanoszone są na podłoże przy pomocy specjalnych urządzeń, w sposób kontaktowy – przy pomocy igieł lub niekontaktowy – np. piezoelektrycznie.
Mikromacierze oligonukleotydowe zbudowane są z 25–70 oligonukleotydowych sond syntetyzowanych metodą fotolitografii bezpośrednio na plastikowej płytce. Metoda fotolitografii polega na specyficznej aktywacji światłem lasera ostatnich nukleotydów syntetyzowanych sond i przyłączaniu żądanych nukleotydów tworzących w ten sposób specyficzną dla danej próby sondę. W przypadku mikromacierzy tego typu gęstość zadruku jest bardzo duża.
Jak przeprowadzić eksperyment z wykorzystaniem mikromacierzy?
Sukces analizy ekspresji genów metodą mikromacierzy DNA uzależniony jest od odpowiedniego zaplanowania eksperymentu.
Pierwszą decyzją, jaką należy podjąć przed rozpoczęciem doświadczenia jest wybór mikromacierzy. Jej rodzaj jest ściśle uzależniony od celu i obiektu badań. Do analizy ekspresji genów używa się mikromacierzy ekspresyjnych, do wykrywania polimorfizmów typu SNP czy aberracji chromosomowych – mikromacierzy do genotypowania.
Kolejnym etapem jest izolacja całkowitego mRNA z badanego materiału biologicznego.
Rodzaje mikromacierzy
• Mikromacierze cDNA
Jeśli stosowane są mikromacierze cDNA, to RNA po izolacji jest przepisywany na komplementarny jednoniciowy DNA, przy pomocy enzymu – odwrotnej transkryptazy (RT-PCR). Do powstających cząsteczek DNA włączane są znakowane nukleotydy – posiadające barwnik fluorescencyjny, co umożliwia późniejszą wizualizację i oszacowanie ilości cząsteczek. Najczęściej używana do znakowania para fluoroforów to Cyanine-3 (Cy-3) i Cyanine-5 (Cy-5), rzadziej stosuje się Alexa555&Alexa647. Jedną z istotnych zalet mikromacierzy cDNA jest to, że znakując dwie próby różnymi barwnikami możemy zbadać i porównać ekspresję genów w próbie eksperymentalnej i kontrolnej – na przykład w zmienionej chorobowo i w zdrowej tkance. Takie dwie próby miesza się i poddaje procesowi hybrydyzacji, podczas którego wyznakowane odcinki cDNA łączą się komplementarnie z sondami na mikromacierzy. Połączone z sondami cDNA fluorochromy, pod wpływem impulsów światła wzbudzanego przez lasery w skanerze emitują falę elektromagnetyczną, która odczytywana jest przez specjalne wysokoczułe detektory i zamieniana na sygnał elektroniczny – obraz, który podlega dalszej analizie. W wyniku skanowania macierzy uzyskuje się oddzielne obrazy dla każdej próby, na których spoty świecą umownymi kolorami na zielono (Cy-3, A555) i na czerwono (Cy-5, A647). Natężenie fluorescencji jest proporcjonalne do liczby ulegających hybrydyzacji do matrycy wyznakowanych cząsteczek (analiza ilościowa). Komputerowe nałożenie obrazu zielonego na czerwony pozwala na wizualizację różnic w ekspresji genów manifestującej się różnymi kolorami punktów (analiza jakościowa). Świecenie spotu na zielono lub na czerwono oznacza, że obserwowana jest aktywność danego genu tylko w jednej z badanych prób. Kolory pośrednie oznaczają, iż gen ulega ekspresji w obydwu badanych próbach. Jeżeli ekspresja w obydwu próbach jest bardzo zbliżona lub taka sama, wtedy obserwujemy punkty w kolorze żółtym. Jeżeli w którejś z prób badany gen ulega wyższej ekspresji niż w drugiej, wtedy pojawia się fluorescencja w kolorze pomarańczowym.
• Mikromacierze oligonukleotydowe</en>
W przypadku chipów znakowany jest nie cDNA, ale tzw. antysensowny RNA. Ma on sekwencje komplementarną do sond oligonukleotydowych umieszczonych na mikromacierzy. W celu jego otrzymania, wyizolowany RNA zostaje przepisany na cDNA, równocześnie liczba analizowanych cząsteczek ulega zwielokrotnieniu. Utworzony cDNA służy jako matryca do transkrypcji in vitro, w czasie której do powstającego cRNA dołączana jest biotyna. Następnie, już po hybrydyzacji, biotynylowany cRNA znakuje się przy pomocy kompleksu streptawidyny z barwnikiem fluorescencyjnym – fikoerytryną. W przypadku mikromacierzy oligonukleotydowych w pojedynczym eksperymencie można hybrydyzować tylko jedną próbę.
Odczyt wyników polega na oddzielnym skanowaniu każdej wyznakowanej jednym fluorochromem płytki i łączeniu wyników z dwóch płytek w dalszej analizie porównawczej.
Tab.1 Porównanie mikromacierzy cDNA i mikromacierzy oligonukleotydowych.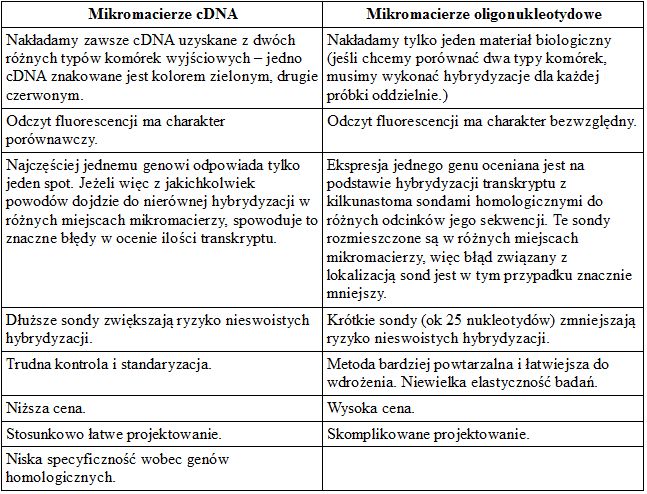
Zastosowanie mikromacierzy
Mikromacierze stosowane są w biologii molekularnej m.in. do badania:
– ekspresji genów,
– metabolizmu obcych dla organizmu substancji,
– cyklu komórkowego,
– stresów, np. oksydacyjny,
– apoptozy, czyli programowanej śmierci komórki,
– polimorfizmów punktowych – SNP (single nucleotide polimorphism),
– aberracji chromosomowych,
– interakcji białko-DNA,
– identyfikacji alternatywnego splicingu,
– metylacji DNA,
– identyfikacji profili mikroRNA, itp.
Mikromacierze DNA odgrywają bardzo ważną rolę w onkologii ponieważ umożliwiają:
– identyfikację zarówno czynników powodujących powstawanie i rozwój nowotworu, jak i mechanizmów obronnych organizmu,
– postawienie odpowiednio wczesnej i prawidłowej diagnozy,
– właściwy dobór terapii,
– poznanie czynników wpływających na skuteczność terapii.
Prowadzone w ostatnich latach badania pokazały jak liczne i różnorodne korzyści przynieść może zastosowanie mikromacierzy DNA. Szczególnie duże nadzieje wiąże się z ich praktycznym wykorzystaniem w medycynie, weterynarii, farmakogenomice (testowanie nowych leków), nutrigenomice czy fitopatologii.
Uważa się, iż chipy DNA umożliwią szybką i precyzyjną diagnostykę wielu chorób, lepsze poznanie ich etiologii i mechanizmu molekularnego oraz bardziej trafny dobór optymalnej terapii.
Autor: Joanna Rusecka
Literatura:
1. „Analiza DNA – teoria i praktyka” pod red. prof. dr hab. Ryszarda Słomskiego; Wydawnictwo Uniwersytetu Przyrodniczego w Poznaniu; Poznań 2011; s.468-473.
2. Sadkowski Tomasz, Motyl Tomasz; 2007; „Mikromacierze DNA – nowe narzędzie badawcze w fizjologii i patologii”; Medycyna Weterynaryjna, 63 (11) Suplement; str. 1421-1426;
3. Kisiel Agnieszka, Skąpska Anna, Markiewicz Wojciech T., Figlerowicz Marek; 2004; „Mikromacierze DNA”; Kosmos – problemy nauk biologicznych; tom 53; str. 295 – 303;
4. Król Magdalena, Pawłowski Karol M., Motyl Tomasz; 2009; „Mikromacierze DNA w onkologii weterynaryjnej”; Medycyna Weterynaryjna, 65 (6); str. 377 – 380;
5. Jarząb Barbara, Gubała Elżbieta, Lange Dariusz; 2004; „Mikromacierze DNA i profil ekspresji genów raka brodawkowego tarczycy”; IV Konferencja Sekcji Endokrynologii Molekularnej PTE; Poznań.

