Kinazy to jedna z największych i najbardziej znaczących rodzin białek. Kodujące je geny stanowią aż 2% genomu wśród organizmów eukariotycznych. Kinazy regulują niemal wszystkie ścieżki biochemiczne i mogą fosforylować do 30% całego proteomu. Ścieżki transdukcji sygnałów, w których uczestniczą kinazy, są w dużej mierze zakonserwowane w przebiegu ewolucji, aż 53 podrodziny tych białek odnaleziono jednocześnie wśród drożdży, robaków, owadów oraz kręgowców (rys. 1)
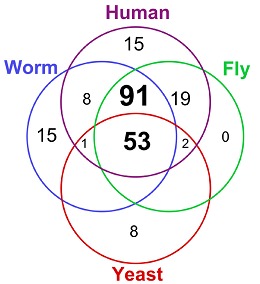
Rys1. Dystrybucja 212 podrodzin kinaz w obrębie 4 organizmów: drożdży Saccharomyces cerevisiae, nicienia Caenorhabditis elegant, muszki owocowej Drosophila melanogaster oraz człowieka.
Substratami, z którymi reagują kinazy, są różnorakie niezliczone białka komórkowe uczestniczące w biochemicznej machinie przekaźnictwa sygnałów wszystkich organizmów żywych. Oddziaływanie kinaz z białkami polega na ich fosforylowaniu, czyli przyłączaniu grupy fosforanowej do ich reszt aminokwasowych. Zmienia to aktywność białek docelowych, lokalizację subkomórkową oraz powinowadztwo do innych białek. Grupa fosforanowa przyłączana do białek przy udziale kinaz pochodzi najczęściej z wysokoenergetycznego związku ATP, jest ona następnie kowalencyjnie przyłączana do jednego z trzech aminokwasów posiadających wolną grupę hydroksylową: seryny, treoniny i tyrozyny. Spotyka się również przedstawicieli kinaz fosforyzujących reszty histydyny.
Z powodu istotnego wpływu na funkcjonowanie komórek, aktywność kinaz musi być wysoce specyficznie regulowana. Są one włączane i wyłączane poprzez fosforyzację (czasem jest to autofosforylacja, gdy kinaza sama reguluje swoją aktywność), przyłączanie specyficznych aktywatorów, inhibitorów i innych małych molekuł, kontrolujących lokalizację kinaz w komórce względem ich substratów.
Podjednostki katalityczne wielu kinaz białkowych są wysoce zakonserwowane, w ich budowie odnaleźć można charakterystyczny rdzeń katalityczny. Na N-końcu domeny katalitycznej występuje fragment łańcucha bogaty w reszty glicyny, zaś w ich sąsiedztwie położona jest reszta lizyny, zaangażowana bezpośrednio w wiązanie ATP. W centralnej części domeny katalitycznej wyróżnia się zakonserwowana reszta kwasu asparaginowego, kluczowa dla katalitycznej aktywności tych enzymów.
Większość kinaz występujących w naturze ma aktywność serynowo-treoninową (EC 2.7.11.1). Fosforylują one wolne grupy –OH reszt seryny i treoniny. Aktywność tej grupy kinaz jest regulowana przez specyficzne wydarzenia, np. uszkodzenia DNA, jak również przez sygnały chemiczne, takie jak cAMP/cGMP, diacylglicerol oraz Ca2+/kalmodulina. Ważną grupę kinaz serynowo-treoninowych stanowią kinazy MAP (mitogen-activated protein kinases), odgrywające rolę w regulacji odpowiedzi na sygnały zewnętrzne dochodzące do komórki (mitogeny), często wywołujące stres oksydacyjny. Mają one wpływ na ekspresję genów, podziały, różnicowanie, ruch i apoptozę komórek. Kinazy MAP są zaangażowane w działania większości pozajądrowych onkogenów. Są odpowiedzialne za odpowiedź komórkową na działanie czynników wzrostu, takich jak BDNF czy NGF. Bodźce działające na komórkę powodują aktywację kaskady MAPK, mającą hierarchiczną strukturę: składają się na nią kinazy klasy MAPK, które z kolei są fosforylowane i aktywowane przez MAPKK, które z kolei są fosforylowane i regulowane przez MAPKKK. MAPKKK są aktywowane w wyniku interakcji z białkami należącymi do rodziny małych białek GTPazowych, takich jak Ras/Rap albo RhoA, bądź innych kinaz. U ssaków zidentyfikowano jak dotąd cztery grupy kinaz MAP:
1. ERK (extracellular signal-regulated kinases) – poprzez kinazy tej grupy działają czynniki wzrostu i estry forbolu; odpowiadają za regulację proliferacji i różnicowania komórek;
2. JNK (c-Jun N-terminal kinases) określane też jako kinazy aktywowane stresem (stress-activated protein kinases, SAPK) – pośredniczą w działaniu czynników stresowych: cytokin, promieniowania ultrafioletowego, szoku cieplnego, szoku osmotycznego, są zaangażowane w różnicowanie komórek i ich apoptozę;
3. Izoformy białka p38 – ich funkcja jest zbliżona do kinaz grupy JNK;
4. ERK5 – niedawno zidentyfikowana grupa kinaz, aktywowanych zarówno działaniem czynników stresowych i czynników wzrostu.
Kinazy tyrozynowe są mniej liczne aniżeli serynowo-treoninowe, katalizują one fosforylację reszt tyrozyny. Do tej rodziny należą enzymy, stanowiące integralną część receptorów katalitycznych, posiadające w swej strukturze zewnątrzkomórkową domenę receptorową, domenę transbłonową oraz wewnątrzkomórkową domenę o aktywności kinazy. Pełnią istotne funkcje w podziałach i różnicowaniu komórek oraz w morfogenezie. W tej grupie wyróżnić można m .in. receptory czynników wzrostowych (płytko pochodny czynnik wzrostu PDGF, receptor insuliny oraz insulinopodobnego czynnika wzrostu IGF1, czynnik wzrostu naskórka EGF). Równocześnie w komórkach występuje liczna grupa cytoplazmatycznych kinaz tyrozynowych, takich jak kinaza Abl oraz kinaza Src.
Rozregulowana aktywność kinaz jest podłożem wielu chorób, w szczególności nowotworów. U źródeł tych zjawisk leżą często zaburzenia w kontroli cyklu i podziałów komórkowych. Obecnie trwają rozwinięte badania nad lekami hamującymi nadmierną aktywność kinaz, za przykład mogą posłużyć takie medykamenty jak Imatinib czy Gefitinib.
Autor: Paweł Burdiak
Bibliografia:
1. Hanks SK (2003). „Genomic analysis of the eukaryotic protein kinase superfamily: a perspective”. Genome Biol. 4 (5): 111.
2. Hanks SK, Quinn AM (1991). „Protein kinase catalytic domain sequence database: identification of conserved features of primary structure and classification of family members”. Meth. Enzymol. 200: 38–62.
3. Hunter T (1991). „Protein kinase classification”. Meth. Enzymol. 200: 3–37.
4. Manning G, Whyte DB. et al. (2002). „The protein kinase complement of the human genome”. Science 298 (5600): 1912–1934.

