Autor: Marcelina Olszak
Uniwersytet Przyrodniczy w Lublinie
Glukozynolany są to roślinne siarkowe glikozydy, które zawierają cząsteczkę β-D-glukozy, siarkę oraz łańcuch boczny o strukturze alifatycznej lub aromatycznej. Różnorodność budowy łańcucha bocznego powoduje, że obecnie znanych jest około 100 różnych związków zaliczających się do tej grupy. Ogólny podział glukozynolanów obejmuje trzy grupy: glukozynolany alifatyczne, w których łańcuch boczny pochodzi od aminokwasów alifatycznych (leucyna, izoleucyna, metionina, walina, alanina), glukozynolany aromatyczne z łańcuchem pochodzącym od aminokwasów o budowie aromatycznej (fenyloalanina, tyrozyna) oraz glukozynolany indolowi – łańcuch boczny zbudowany na bazie tryptofanu. Związki te występują przede wszystkim w roślinach z rodziny Brassicacea, czyli między innymi w: kapuście białej, włoskiej, czerwonej, pekińskiej oraz brukselskiej, jak również w rzepaku, kalafiorze, brokule, rzodkiewce, kalarepie, rukoli, chrzanie i gorczycy.
| Występowanie | Glukozynolany i produkty ich rozpadu |
| Brokuły | glukobrassycyna, glukorafanina, glukoiberyna, neoglukobrassycyna, nitryl sulforafanu, sulforafan, brucyna, iberyna |
| Kapusta biała | synigryna, glukobrassycyna, 3,3’-diindolilometan, indol-3-karbinol, askorbigen, izotiocyjanianfenyloetylu, izotiocyjanian allilu |
| Kalafior | glukobrassycyna, synigryna,progoitryna, izotiocyjanian allilu, glukonapina, indol-3-karbinol |
| Brukselka | neoglukobrassycyna, synigryna, glukobrassycyna, glukoiberynaprogoitryna, glukonapina, glukorafanina |
Najczęściej spotykanymi glukozynolami w roślinach kapustnych są: synigryna, glukobrassicyna, glukonapina, progoitryna, glukoiberyna, noeglukobrassicyna oraz glukorafanina. Pod względem budowy chemicznej są to stabilne związki, które mogą występować w różnych formach chemicznych oraz w różnej ilości. Są to związki odporne na działanie wysokiej temperatury, natomiast łatwo ulegają hydrolizie, zarówno enzymatycznej jak i nieenzymatycznej. Enzymem biorącym udział w tym procesie jest mirozynaza (β-tioglukozydaza, glukohydrolazatioglukozydowa EC 3.2.3.1). Enzym ten występuje w tkankach roślin kapustnych i uwalniany jest w przypadku uszkodzenia komórek roślinnych, miażdżenia oraz innych procesów technologicznych. W wyniku hydrolizy enzymatycznej powstaje glukoza, jon siarczanowy oraz inne produkty degradacji zależne od warunków środowiska, głównie pH. Ważną cechą produktów degradacji jest ich wysoka aktywność biologiczna, szczególnie w przypadku oddziaływań szkodnik-roślina.
Hydroliza glukozynolanów jest prawdopodobnie reakcją dwuetapową. Pierwsza faza – glikozylacja polega na kowalencyjnyn wiązaniu mirozynazy z resztą glukozy glukozonolanu. W trakcie tego etapu następuje również uwolnienie aglikonu. Drugi etap nazywany deglikozylacją polega na uwolnieniu glukozy przy udziale cząsteczki wody oraz na regeneracji enzymu.
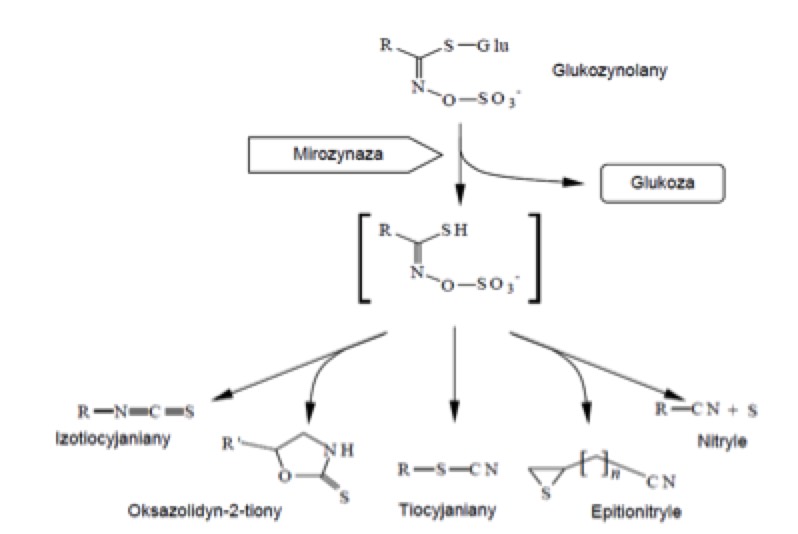
Rys. Rozkład glukozynolanów przy udziale enzymu mirozynazy oraz produkty ich hydrolizy. R- rodnik
Zawartość tych związków różni się w zależności od odmiany rośliny. Mają na nią wpływ warunki uprawy takie jak klimat, dostępność składników odżywczych oraz termin zbioru. Zawartość różni się w poszczególnych częściach rośliny, natomiast szczególnie obficie występują w nasionach. Ma to szczególnie duże znaczenie w przypadku rolnictwa ekologicznego lub zintegrowanego, ponieważ obniżenie stosowania chemicznych środków ochrony roślinzwiększa możliwość inwazji patogenów.
Na zawartość glukozynolanów w roślinach mają wpływ następujące czynniki abiotyczne:
• niedobór wody – zawartość glukozynolanów spada, ponieważ ograniczeniu ulega pobieranie siarki przez roślinę, pierwiastka biorącego udział w syntezie tych związków,
• nadmiar wody – z powodu bujnego wzrostu roślin następuje efekt rozcieńczenia glukozynolanów w roślinie, może wystąpić również wymywanie siarki z korzeni,
• nawożenie siarką – największy wpływ tego pierwiastka obserwowany jest po 6 tygodniach od zastosowania nawozu, prawdopodobnie jest to okres potrzebny, aby siarka stała się dostępna dla rośliny.
Obecność glukozynolanów w żywności nadaje jej charakter funkcjonalny oraz prozdrowotny. Ponadto związki te nazywane są naturalnymi pestycydami, ponieważ chronią rośliny przed trawożernymi zwierzętami, insektami i patogenami. Produkty ich katabolizmu wykazują toksyczność w stosunku do wielu grzybów patogennych, wirusów, bakterii, owadów i roślin wyższych. Pełnią one funkcje atraktantów, repelentów lub związków, które modyfikują zachowanie szkodników, mogą również uczestniczyć w oddziaływaniach allelopatycznych. Co więcej niektóre produkty hydrolizy glukozynolanów działają przeciwwirusowo, przeciwgrzybiczo i przeciwbakteryjnie w stosunku do ludzkich patogenów np. Helicobacter pylori. Zainteresowanie tymi związkami wynika także z faktu, że są to substancje antyżywieniowe, ponieważ obniżają wartość wytłoków wysokobiałkowych lub śruty poekstrakcyjnej uzyskiwanej z nasion rzepaku. Ponadto rośliny krzyżowe ze względu na ich specyficzny smak i zapach są stosowane jako warzywa i przyprawy. Związane jest to z obecnością izotiocyjanianów – produktów katabolizmu glukozynolanów.
Wykazane zostało również, że glukozynolany występujące w warzywach kapustnych odgrywają istotną rolę w chemioprewencji nowotworów. Jedną ze strategii proponowanych w profilaktyce chorób nowotworowych jest zapobieganie powstawaniu nowotworów na skutek spożywania nietoksycznych związków. Naturalne substancje, które występują w roślinach mogą jedynie zablokować i zapobiec kancerogenezie na wczesnych jej etapach. Mniejszy wpływ obserwowany jest na późniejsze etapy nowotworzenia. Zarówno badania in vitro jak i in vivo wykazały, że najsilniejsze właściwości przeciwnowotworowe posiadają izotiocyjaniany oraz indole: izotiocyjanianfenyloetylu, sulforafan i indolo-3- karbinol oraz produkt jego kondensacji 3,3’-diindolilometan.
Glukozynolany działają przeciwnowotworowo poprzez:
• indukowanie ekspresji enzymów fazy II,
• inhibicję enzymów fazy I, które są odpowiedzialne za aktywację metaboliczną kancerogenów,
• blokowanie czynników uszkadzających DNA,
• ograniczanie transformacji komórek zainicjowanych,
• udział w metabolizmie estrogenów,
• przywrócenie apoptozy – zaprogramowanej śmierci komórek rakowych.
Oprócz wielu korzyści glukozynolany mogą powodować również działania niepożądane. Spożywane w nadmiernych ilościach wykazują właściwości wolotwórcze (goitrogenne), a nawet mutagenne. Duże ilości roślin kapustnych w diecie mogą powodować spadek aktywności sekrecyjnej tarczycy na skutek zahamowania syntezy tyroksyny. Konsekwencją tego zjawiska jest obniżenie poziomu trijodotyroniny (T3) i tetrajodotyroniny (T4) we krwi, a następnie wzrost aktywności tyreotropowej przysadki mózgowej. Zmiany te prowadzą do przerostu masy tarczycy – wole. Zagrożenie działania czynników goitrogennych maleje w przypadku prawidłowej i zbilansowanej diety. Silniejsze działanie obserwowane jest przy mniejszej podaży jodu w diecie. Ważne jest więc, aby spożywaniu warzyw kapustnych towarzyszyła obecność w pożywieniu jodu. Dieta odgrywa więc istotną rolę w profilaktyce nowotworowej. Jej modyfikacja poprzez dostarczenia związków biologicznie czynnych indukuje odpowiednie poziomy ochronne, co staje się obiecującą strategią w profilaktyce chorób nowotworowych.
Literatura:
1. Kwiatkowska E., Bawa S.: Glukozynolany w profilaktyce chorób nowotworowych – mechanizmy działania. Roczn. PZH, 58, NR 1, 7-13, 2007.
2. Oleszek W.: Glukozynolany – występowanie i znaczenie ekologiczne. Wiadomości Botaniczne, 39 (1/2): 49-58, 1995.
3. Sosińska E., Obiedziński M.W.: Badania nad bioaktywnymi glukozynolanami w wybranych odmianach warzyw krzyżowych techniką HPLC. Żywność. Nauka. Technologia. Jakość, 5 (54), 129 – 136, 2007.
4. Szwejda-Grzybowska J.: Antykancerogenne składniki warzyw kapustnychi ich znaczenie w profilaktyce choróbnowotworowych. Bromat. Chem. Toksykol. – XLIV, 4, 1039–1046, 2011.
5. Śmiechowska A., Bartoszek A., Namieśnik J.: Przeciwrakotwórcze właściwości glukozynolanówzawartych w kapuście (Brassicaoleraceavar. capitata) oraz produktów ich rozpadu. PostepyHigMedDosw. (online), 62: 125-140, 2008.
6. Troczyńska J.: System mirozynaza – glukozynolany — charakterystyka i funkcje w roślinie. Rośliny Oleiste – OilseedCrops, Tom XXVI, 51-64, 2005.

