PRZEDRUK, oryginał dostępny pod adresem www
Fragment skryptu: Preparatyka związków organicznych. Przepisy do ćwiczeń
Uniwersytet Jagielloński (www)
Wydział Farmaceutyczny Collegium Medicum (www)
Katedra Chemii Organicznej (www)
Kierownik: Prof. UJ, dr hab. Marek Cegła
Adres:
ul. Medyczna 9
30-688 Kraków
Kontakt: tel. 012 620 55 00
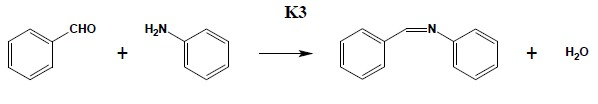
Odczynniki:
Aldehyd benzoesowy 3 cm3
Anilina 3 cm3
3 cm3 aldehydu benzoesowego i 3 cm3 aniliny ogrzewa się do wrzenia w kolbie okrągłodennej o pojemności 50 cm3 pod chłodnicą zwrotną przez 1 godzinę. Następnie mieszaninę reakcyjną przenosi się szybko (możliwość skrzepnięcia w kolbie) do małej zlewki, chłodzi, umieszczając zlewkę w misce wypełnionej mieszaniną wody z lodem, pocierając jednocześnie o ścianki zlewki bagietką szklaną. Wydzielony osad odsącza się na lejku Büchnera. Surowy produkt krystalizuje z 70% etanolu. (otrzymany w trakcie krystalizacji nasycony roztwór benzylidenoaniliny, po przesączeniu na gorąco przez sączek karbowany, należy szybko ochłodzić w lodzie, energicznie mieszając i pocierając o ścianki zlewki bagietką szklaną, dla uniknięcia powstawania oleju i przyśpieszenia wypadania benzylidenoaniliny) Czysta benzylidenoanilina topi się w 52oC.
Benzylidenoalinina jest lotna z parą wodną co można również wykorzystać dla jej oczyszczenia (w trakcie destylacji należy destylat zbierać do naczynia chłodzonego w lodzie).
Uwaga1. Anilina jest trucizną. Działa szkodliwie na układ nerwowy i krwionośny.
Uwaga2. Aldehyd benzoesowy. Działa szkodliwie po połknięciu.
Uwaga3. Etanol jest substancją wysoce palną.
Uwaga4. Przesącz powstały po reakcji i po krystalizacji zlać do butelki z napisem Zlewki etanolowe.

