Glikoliza (gr. „glik” – słodki i „lysis” – rozpuszczanie) jest łańcuchem reakcji prowadzącym do przekształcenia glukozy w pirogronian. Zachodzi ona w cytoplazmie prawie wszystkich organizmów żywych i służy do wytwarzania energii zgromadzonej w ATP oraz do dostarczania elementów budujących składniki komórki. U tlenowców stanowi zaledwie wstępny etap oddychania tlenowego.
Glikoliza składa się z dziesięciu reakcji i można ją podzielić na dwie fazy. Pierwsza z nich przekształca glukozę w fruktozo-1,6-bisfosforan i wymaga zużycia dwóch cząsteczek ATP na każdą cząsteczkę cukru.
W drugim etapie zachodzi rozszczepienie fruktozo-1,6-bisfosforanu na dwa związki, ulegające wzajemnym przekształceniom. Jeden z nich, aldehyd 3-fosfoglicerynowy, ulega dalszym przemianom obejmującym utlenianie i fosforylację, a reakcjom tym towarzyszy utworzenie ATP.
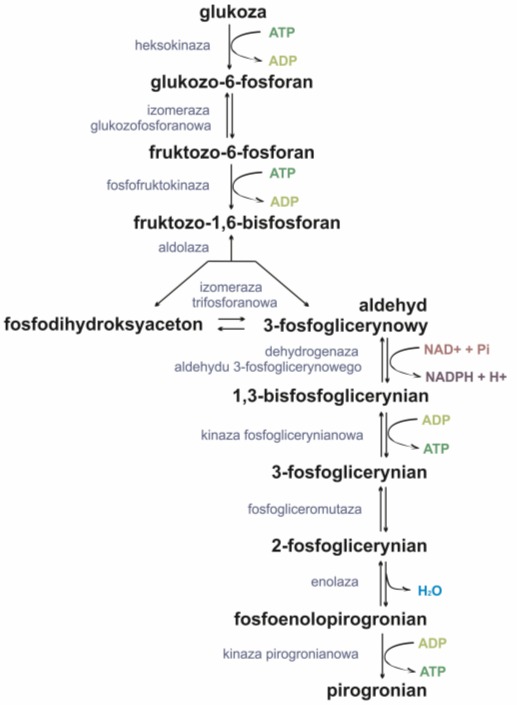
Rys. 1. Glikoliza
Reakcja sumaryczna glikolizy jest następująca:
Glukoza + 2Pi + 2ADP + NAD+ -> 2 cząsteczki pirogronianu + 2 ATP + 2NADH + 2H+ 2H2O
Podczas przekształcania glukozy w dwie cząsteczki pirogronianu powstają zatem dwie cząsteczki ATP.
Tabela. 1. Zużycie i synteza ATP podczas glikolizy
Akceptorem elektronów podczas procesu utleniania aldehydu 3-fosfoglicerynowego jest NAD+, który musi być regenerowany, aby umożliwić stałe zachodzenie przemian glikolitycznych. Organizmy tlenowe wykorzystują do tego łańcuch oddechowy, podczas którego NADH przekazuje elektrony na tlen. W warunkach beztlenowych NADH redukuje pirogronian do mleczanu lub etanolu w procesach tak zwanej fermentacji mlekowej lub alkoholowej.
W warunkach fizjologicznych rekcje glikolizy są odwracalne. Wyjątek stanowią trzy procesy katalizowane przez heksokinazę, fosfofruktokinazę i kinazę pirogronianową. Najważniejszym punktem kontrolnym glikolizy jest reakcja regulowana przez fosfofruktokinazę, aktywną w sytuacji dużego zapotrzebowania na energię lub składniki budulcowe, tzn. w obecności AMP i fruktozo-2,6-bisfosforanu, sygnalizującyego duże stężenie glukozy w wątrobie. Hamują ją natomiast duże stężenia ATP i cytrynianu. Brak aktywności tego enzymu przyczynia się do akumulowania glukozo-6-fosforanu inaktywującego heksakinazę.
Ostatni etap kontrolny to reakcja kinazy pirogronianowej allosterycznie hamowanej przez ATP i alaninę, a aktywowanej przez fruktozo-1,6-bisfosforan. Małe stężenie glukozy we krwi pobudza fosforylację tego enzymu w wątrobie i hamuje tym samym jego aktywność oraz zużycie glukozy.
Do szlaku glikolitycznego mogą wejść również inne, powszechnie występujące monosacharydy, np. fruktoza, która powstaje w wyniku rozpadu sacharozy, czyli cukru spożywczego. Jej przemiany zachodzące w wątrobie określa się mianem szlaku przemian fruktozo-1-fosforanu.
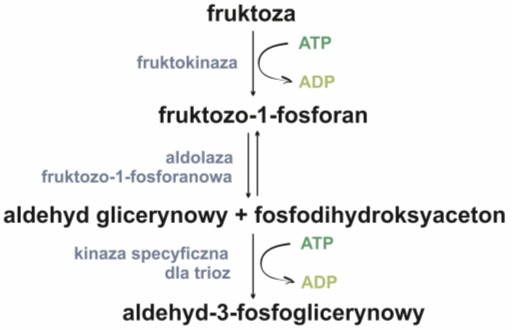
Rys. 2. Szlak przemian fruktozo-1-fosforanu
Glikolizie może ulegać również galaktoza, będąca jednym ze składników laktozy – cukru występującego w mleku. Podczas czterech kolejnych etapów ulega ona przekształceniu w glukozo-6-fosforan. Sumaryczną reakcję katalizowaną przez galaktokinazę można zapisać równaniem:
Galaktoza + ATP -> glukozo-1-fosforan + ADP + H+
Glukozo-1- fosforan ulega następnie izomeryzacji do glukozo-6-fosforanu, a przemiana ta jest katalizowana przez enzym fosfoglukomutazę.
Znana jest niewielka liczb chorób, w których stwierdzono brak aktywności enzymów glikolitycznych. Ich zasadniczym objawem jest niedokrwistość hemolityczna. W intensywnie rosnących komórkach nowotworowych glikoliza przebiega znacznie szybciej, niż tego wymaga cykl Krebsa. Produkcja pirogronianu przewyższa zdolności jego metabolizowania, co prowadzi do nadmiernego wytwarzania mleczanu i zakwaszania środowiska w guzie.
Autor: Anna Kurcek
Literatura:
• Lubert Stryer „Biochemia”, Wydawnictwo Naukowe PWN, Warszawa 2003;
• Robert K. Murray, Daryl K. Granner, Peter A. Mayes, Victor W. Rodwell “Biochemia Harpera” Wydanie III, Wydawnictwo Lekarskie PZWL, Warszawa 1995.

