PRZEDRUK, oryginał dostępny pod adresem www
Fragment skryptu: Biologia molekularna roślin
Uniwersytet Warszawski (www)
Instytut Biochemii i Biofizyki PAN (www)
Zakład Biologii Molekularnej Roślin (www)
Kierownik Zakładu: Prof. dr hab. Andrzej Jerzmanowski
Adres:
ul. Pawińskiego 5a,
02-106 Warszawa
Kontakt: tel. (+48 22) 592 5704,
E-mail: andyj@ibb.waw.pl
Zakład Biologii Molekularnej Roślin
Problematyka badawcza: Rola struktury chromatyny w regulacji rozwoju roślin oraz w odpowiedzi na czynniki stresowe i hormonalne. Prowadzone aktualnie badania mają na celu poznanie funkcji roślinnych kompleksów remodelujących chromatynę, histonu H1 i modyfikacji potranslacyjnych histonów rdzeniowych, a także opisanie proteomu jądrowego rośliny modelowej Arabidopsis thaliana.
Stosowane techniki: Większość metod biologii molekularnej, metody biochemii białek, analiza proteomiczna (mass-spec) i transkryptomiczna (mikromacierze), genetyka Arabidopsis thaliana (konstrukcja i analiza mutantów), metody bioinformatyczne.
_______________________________________________________________________________
Badanie oddziaływań białek – drożdżowy system dwuhybrydowy
Drożdżowy system dwuhybrydowy (ang. Yeast Two Hybrid) służy do badania oddziaływań między dwoma potencjalnymi partnerami białkowymi. W technice tej wykorzystuje się fakt, że wiele eukariotycznych czynników transkrypcyjnych zawiera dwie funkcjonalnie niezależne domeny. Jedna z nich wiąże się z DNA (BD, ang. Binding Domain), druga natomiast aktywuje transkrypcję danego genu (AD, ang. Activation Domain). Obie te domeny są zatem niezbędne aby nastąpiła transkrypcja określonego genu. W drożdżowym systemie dwuhybrydowym każda z tych domen zostaje połączona z jednym z potencjalnych i będących przedmiotem badań, partnerów białkowych. W efekcie powstają dwa tzw. białka fuzyjne: jedno z nich związane z domeną wiążącą się z DNA (BD), drugie zaś z domeną aktywującą transkrypcję (AD).
Geny kodujące oba fuzyjne białka znajdują się na dwóch różnych plazmidach. Plazmidy te wprowadza się do komórek drożdży, zatem oba białka podlegają ekspresji w tej samej komórce. Jeżeli badane białka oddziałują ze sobą, obie domeny: aktywująca transkrypcję (AD) i wiążąca się z DNA (BD), zbliżają się do siebie na tyle blisko, by móc aktywować transkrypcję konkretnego genu. W opisywanym układzie genem, który ulega transkrypcji jest jeden z genów reporterowych, np. gen kodujący β-galaktozydazę (lac-Z) lub HIS3.
Metoda dwuhybrydowa polega na wykorzystaniu dwudomenowej struktury białka, aktywatora GAL-4. Aktywator ten składa się z domeny aktywującej transkrypcję genu i z domeny wiążącej się do rejonu promotorowego – UAS genu GAL1. Genem reporterowym jest lacZ. Używane są dwa wektory, które po wprowadzeniu do komórek drożdży dają dwa białka fuzyjne w dwóch niezależnych układach:
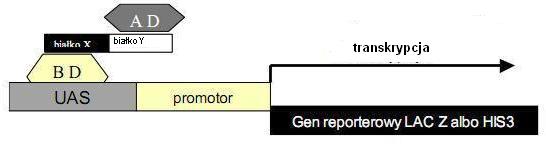
Rys. 1 Schemat działania drożdżowego systemu dwuhybrydowego.
– pGAD424 zawierający domenę aktywującą (AD) i sekwencję kodującą białko FCA oraz pGBT9 zawierający domenę wiążącą się z DNA (BD) i sekwencję kodującą drugie białko AtSWI3B.
– pGAD424 zawierający domenę aktywującą (AD) i sekwencję kodującą białko AtSWI3B oraz pGBT9 zawierający domenę wiążącą się z DNA (BD) i sekwencję kodującą białko FCA.
Jeśli białko X oddziałuje z białkiem Y, gen reporterowy kodujący β-galaktozydazę ulegnie transkrypcji (Rys. 1). Wówczas aktywne białko β-galaktozydazy w obecności podanego z zewnątrz substratu, którym jest X-gal (5-bromo-4-chloro- 3-indolilo-β-D-galaktopiranozyd) przeprowadzi reakcję, w wyniku której powstanie niebieski produkt.
System dwuhybrydowy może być wykorzystywany jako metoda ilościowa. To znaczy można oceniać siłę oddziaływań, a nie tylko stwierdzać ich obecność lub brak. Metoda ilościowa jest wykorzystywana bardzo rzadko, z uwagi na liczne ograniczenia wynikające m. in. z różnic w produkcji białka między poszczególnymi koloniami drożdżowymi, a także różnic w tolerowaniu danego białka przez komórkę drożdżową np. toksyczność białek. Ograniczenia te mogą powodować niedokładności w wynikach.
Schemat metody ilosciowej: (należy ustalić takie same ilości białka we wszystkich próbkach
– Pomiar gęstości komórek drożdżowych (spektrofotometr)
– Pomiar ilości białka (metoda Bradford)
– Badanie aktywności β-galaktozydazy poprzez pomiar ilości barwnego produktu na płytkach wielodołkowych (czytnik spektrofotometryczny)
Zastosowanie systemu dwuhybrydowego
Drożdżowy system dwuhybrydowy można używać zarówno do badania kierunkowych oddziaływań między dwoma białkami, jak również do poszukiwania nowych, nieznanych partnerów danego białka. W pierwszym przypadku należy skonstruować dwa plazmidy, z których eksprymowane będą dwa białka fuzyjne: jedno z domeną aktywującą, zaś drugie z domeną wiążącą. Używając odpowiednich starterów z zaprojektowanymi miejscami cięcia przez enzymy restrykcyjne należy wykonać reakcję PCR na matrycy cDNA. Otrzymane fragmenty DNA trzeba następnie zligować z odpowiednio przygotowanymi plazmidami, jednym kodującym domenę wiążącą, a drugim – domenę aktywującą, pamiętając o zachowaniu właściwej ramki odczytu. Po uzyskaniu właściwych plazmidów należy stransformować nimi odpowiedni szczep drożdży, np. Y190, HF7c czy CG-1945, które mają uszkodzony szlak syntezy leucyny i tryptofanu i potrzebują tych aminokwasów do wzrostu.
Po transformacji dwoma plazmidami drożdże wysiewa się na odpowiednią pożywkę selekcyjną. Uzyskane kolonie przeszczepia się na nową szalkę i następnie przeprowadza się test dwuhybrydowy.
Drugim zastosowaniem drożdżowego systemu dwuhybrydowego jest poszukiwanie nieznanych partnerów konkretnego białka. W tym celu można przeszukiwać całą bibliotekę cDNA w określonym wektorze z domeną aktywującą za pomocą interesującego nas białka, wyrażanego z plazmidu z domeną wiążącą. Zarówno plazmid kodujący białko będące „przynętą” (ang. Bait plasmid) którego partnerów chcemy poznać, jak i całą bibliotekę cDNA tworzy się w analogiczny sposób jak w przypadku kierunkowego systemu dwuhybrydowego. Przy przeszukiwaniu biblioteki łatwiej jest przeprowadzić wstępną selekcję ewentualnych partnerów badanego białka przed właściwym testem na obecność β-galaktozydazy. W wielu systemach wykorzystuje się zatem obecność drugiego genu reporterowego, tym razem pokarmowego, np. genu HIS3, kodującego enzym niezbędny w szlaku biosyntezy histydyny.
Ponieważ transformacje pojedynczymi plazmidami są wydajniejsze od transformacji podwójnych, można też najpierw stransformować drożdże plazmidem kodującym „przynętę”, wysiewając je na odpowiednie podłoże selekcyjne i po uzyskaniu komórek zawierających jeden plazmid wprowadzić do nich plazmidy biblioteki. Po wstępnej selekcji na podłożu bez histydyny wyrosną kolonie, w których nastąpiła aktywacja transkrypcji genu HIS3. Dopiero na tych koloniach należy przeprowadzić test na obecność β-galaktozydazy w komórkach drożdży. Dzięki tej metodzie można stosunkowo szybko wykryć nowych partnerów białkowych dla interesującego nas białka. Ponadto, należy podkreślić, iż w systemie dwuhybrydowym możliwe jest badanie oddziaływań między białkami, które normalnie występują w komórce w małych ilościach, zatem trudno je sprawdzić innymi metodami, zaś w drożdżach białka fuzyjne eksprymowane z plazmidów wystąpią w ilości wystarczającej do wykonania testu.
Ograniczenia systemu dwuhybrydowego
Główną wadą systemu dwuhybrydowego jest fakt, iż z różnych przyczyn oddziaływań niektórych klas białek nie można zbadać za jego pomocą. Z pewną częstotliwością pojawiają się wyniki fałszywie pozytywne i fałszywie negatywne.
Te pierwsze są najczęściej powodowane przez białka, które, kodowane przez plazmid z domeną wiążącą, są aktywatorami transkrypcji i do aktywacji genu reporterowego nie potrzebują oddziaływania z drugim białkiem fuzyjnym zawierającym domenę aktywującą. Z tego powodu biblioteki cDNA tworzone do przeprowadzania wysokowydajnych analiz dwuhybrydowych są prawie zawsze tworzone w plazmidach kodujących domenę aktywującą, aby białka będące aktywatorami transkrypcji nie powodowały fałszywych wyników pozytywnych. Poza tym zdarzają się też oddziaływania niespecyficzne których wynikiem jest aktywacja genu reporterowego. Ich przyczyny mogą być różne. Niektóre białka fuzyjne z domeną aktywującą mogą oddziaływać z białkiem drożdżowym zawierającym domenę wiążącą i w ten sposób aktywować transkrypcję u drożdży. Analogicznie, białko fuzyjne z domeną wiążącą może, poprzez oddziaływanie z drożdżowym białkiem z domeną aktywującą, aktywować transkrypcję u drożdży. Te dwa przypadki fałszywie pozytywnych wyników systemu dwuhybrydowego można wyeliminować, stosując odpowiednie kontrole negatywne.
W tym celu równolegle do transformacji drożdży plazmidami kodującymi białka fuzyjne należy przeprowadzić transformację plazmidem kodującym białko fuzyjne z domeną-AD z pustym plazmidem kodującym domenę-BD lub kodującym inne białko fuzyjne o którym wiadomo że nie oddziałuje z badanym białkiem fuzyjnym. Analogicznie należy przeprowadzić kontrolę dla białka fuzyjnego z domeną-BD, kotransformując drożdże plazmidem je kodującym wraz z plazmidem-AD pustym bądź kodującym białko które nie oddziałuje z białkiem z domeną-BD. Jeżeli kontrola negatywna zabarwi się na niebiesko, wiadomo, że mamy do czynienia z wynikiem fałszywie pozytywnym. Istnieje również przypadek artefaktu systemu dwuhybrydowego, którego nie da się wyeliminować stosowaniem kontroli negatywnych. Zdarza się on wtedy, gdy oba białka fuzyjne eksprymowane w drożdżach wprawdzie nie oddziałują ze sobą, ale oddziałują z tym samym białkiem drożdżowym i stąd ich domeny aktywująca i wiążąca mogą się znaleźć na tyle blisko siebie, aby aktywować transkrypcję w drożdżach. Z powodu tej możliwości oddziaływania między dwoma białkami stwierdzone w systemie dwuhybrydowym należy jeszcze potwierdzić drugą, niezależną metodą.
Oprócz wyników fałszywie pozytywnych, w systemie dwuhybrydowym zdarzają się również wyniki fałszywie negatywne, tzn. pomimo istnienia oddziaływań nie zostają one wykryte. Tego rodzaju przypadków nie da się wyeliminować stosowaniem kontroli, a spowodowane są one najczęściej niestabilnością danego białka w drożdżach. Poza tym, niektóre białka mogą przybierać w drożdżach niewłaściwą konformację, przez co ich domena wiążąca będzie ukryta i do oddziaływań nie dojdzie. Również niektóre klasy białek, a w szczególności białka błonowe zawierające hydrofobową domenę transbłonową, mogą nie trafić do jądra i wówczas nie dojdzie do aktywacji transkrypcji. Czasami przyczyną otrzymywania wyników fałszywie pozytywnych i fałszywie negatywnych może być też nieprawidłowa hodowla drożdży: zbyt stare drożdże wykazują tendencję do powodowania wyników pozytywnych w teście na obecność β-galaktozydazy. Szczególnie ważne jest również utrzymywanie stabilnej temperatury hodowli drożdży. Z tego powodu wyniki otrzymane w systemie dwuhybrydowym należy potwierdzić za pomocą innych metod, jak np. koimunoprecypitacja (Co-IP). Technika ta polega na dodaniu do mieszaniny obu analizowanych białek, przeciwciała skierowanego przeciwko jednemu z nich.
Jeżeli białka te oddziałują ze sobą można „wyciągnąć” (za pomocą jednego przeciwciała) jednocześnie oba białka (białko wiążące się z przeciwciałem oraz białka, które oddziałują z pierwszym białkiem). Jeśli badane białka nie oddziałują ze sobą, można „wyciągnąć” tylko jedno białko.

