Autor: Anna Kurcek
Hybrydyzacja to zjawisko spontanicznego parowania się zasad pochodzących z różnych nici kwasów nukleinowych. Może zachodzić pomiędzy dwiema cząsteczkami DNA, RNA lub DNA i RNA, o całkowitej lub częściowej komplementarności. Stabilność przyłączonych odcinków zależy od ilości zasad tworzących wiązania.
Na drodze klonowania lub syntezy chemicznej otrzymuje się fragmenty kwasów nukleinowych zwane sondami molekularnymi. Mają one ściśle określoną sekwencję nukleotydową i są łączone z innymi cząsteczkami związanymi na filtrze lub znajdującymi się w preparatach cytologicznych i histologicznych. Podstawową cechą hybrydyzacji jest specyficzność wykorzystywanych sond. Można je projektować samodzielnie, po uprzednich analizach badanego materiału genetycznego. Jednak ze względu na ich dużą dostępność rozwiązanie to stosuje się jedynie w ostateczności.
Wśród obecnie stosowanych sond molekularnych wyróżnia się cztery podstawowe rodzaje:
• dwuniciowe sondy DNA,
• jednoniciowe sondy DNA,
• jednoniciowe sondy oligonukleotydowe (o długości 15-50 nukleotydów),
• jednoniciowe sondy RNA.
Sondy molekularne są odpowiednio wyznakowane, dzięki czemu z łatwością można wykryć komplementarne do nich fragmenty kwasów nukleinowych:
• radioaktywne – izotopami 3H, 32P, 35S, 14C oraz 125I, wykrywanymi dzięki autoradiografii, to pierwsza ze stosowanych metod;
• fluorescencyjne – świecące po wzbudzeniu światłem o określonej długości fali;
• biotynowane – wykrywane za pomocą reakcji awidyna – biotyna;
• wyznakowane antygenowo – wykrywane z użyciem znakowanych przeciwciał;
• z wykorzystaniem barwnych reakcji enzymatycznych.
Istnieje kilka sposobów na wyznakowanie sondy:
• z wykorzystaniem metody PCR i jednym wyznakowanym nukleotydem;
• nick translacja – DNaza I wycina fragment nici DNA, a polimeraza DNA I usuwa nukleotydy w kierunku 5’ do 3’ i syntezuje nową nić. Wykorzystuje do tego umieszczone w preparacie nukleotydy, z których jeden jest wyznakowany;
• random printing, czyli metoda oligoznakowania – stosowana do oznaczania zarówno długich jak i krótkich fragmentów. Klenowa polimeraza DNA syntetyzuje komplementarną nić od końca 3’ dołączonego heksanukleotydu. Reakcja ta zachodzi w obecności jonów Mg2+;
• z użyciem transkrypcji DNA in vitro.
Wykorzystywane w biologii molekularnej metody hybrydyzacyjne pozwalają na umiejscowienie w cząsteczce DNA określonych sekwencji oraz na porównanie różnych fragmentów kwasów nukleinowych pochodzących z tego samego lub z różnych organizmów. Za ich pomocą można także wykrywać powstałe w cząsteczce DNA zmiany.
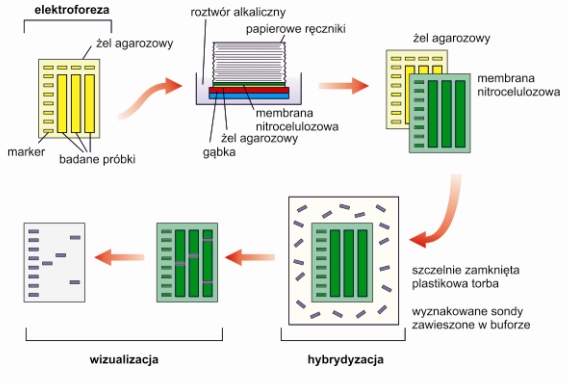
Rys. Ogólny schemat wykonania niektórych metod hybrydyzacyjnych -Southern Blotting, Northern Blotting i DNA fingerprinting; opis w tekście
Do metod hybrydyzacyjnych należą:
Southern Blotting – służy do lokalizacji konkretnej sekwencji DNA po elektroforezie. Na drodze dyfuzji DNA przenoszone jest z żelu na membranę nitrocelulozowa lub nylonową. Inkubuje się ją ze znakowanymi izotopowo sondami komplementarnymi z poszukiwanym fragmentem, który następnie uwidacznia się na zdjęciu rentgenowskim.
Northern Blotting – czyli elektroforetyczno – hybrydyzacyjna detekcja transkryptów. Służy do poszukiwania sekwencji RNA i badania aktywności pojedynczych genów. Wykorzystuje się w niej sondy DNA wyznakowane radioaktywnie.
DNA fingerprinting, czyli metoda genetycznych odcisków palców – wyizolowane DNA trawi się odpowiednimi enzymami restrykcyjnymi, a następnie poddaje elektroforezie i przenosi na filtr nitrocelulozowy, gdzie łączą się z radioaktywnie wyznakowanymi sondami. W ten sposób otrzymuje się „genetyczne odciski palców”, czyli charakterystyczny dla danego osobnika układ pasków DNA.
Hybrydyzacja in situ (ang. in situ hybridization ISH)
Z łac. in situ – w miejscu naturalnego występowania. Znakowany polipeptyd tworzy hybrydę z komplementarnymi sekwencjami znajdującego się w komórce kwasu nukleinowego. Metoda ta pozwala wykryć poszukiwaną sekwencję oraz zlokalizować jej położenie w komórce i na chromosomie. Wykonuje się ją bezpośrednio na szkiełku podstawowym po uprzedniej denaturacji DNA chromosomowego oraz sondy dla uzyskania form jednoniciowych (wysoka temperatura, formamid). Preparat oczyszcza się z białek, a w przypadku stosowania sond DNA należy również uprzednio strawić go RNazą. Niezhybrydyzowane lub słabo zhybrydyzowane fragmenty zostają wypłukane przed uwidocznieniem.
Fluorescencyjna hybrydyzacja in situ (ang. fluorescent in situ hybridization FISH)
Za pomocą wyznakowanej fluorescencyjnie sondy oligonukleotydowej wykrywane są określone sekwencje DNA w badanym materiale. Najczęściej stosowane fluorochromy:
• FITC – (izotiocyjanian fluoresceiny) – zielona fluorescencja;
• TRITC – (izotiocyjanian tetrametylorodaminy) – czerwona fluorescencja;
• AMCA – (amino-methylcoumarin-acetic acid) – niebieska fluorescencja.
Dzięki kombinacjom tych trzech fluorochromów można uzyskać większą liczbę barw. Aby określić położenie sygnału stosuje się kontrastowe barwienie jądra i chromosomów. Przed wykonaniem analizy należy przeprowadzić wstępne badania określające wielkość autofluorescencji badanej próbki. W tym celu wykonuje się hybrydyzację bez sondy lub z użyciem sondy nonsensownej (ang. nonsense probe).
Wielokolorowa FISH (ang. multicolor FISH))
Dzięki wyznakowaniu sond różnymi fluorochromami pozwala na jednoczesne uwidocznienie różnych sekwencji DNA lub różnicowanie chromosomów (sondy malujące).Wykorzystywana jest w diagnostyce zaburzeń chromosomowych towarzyszących określonym chorobom człowieka.
FISH na rozciągniętych włóknach chromatynowych (ang. fiber FISH)
Przed hybrydyzacją przeprowadza się rozciąganie genomowego DNA izolowanego z jąder interfazowych.
Genomowa hybrydyzacja in situ (ang. genomic in situ hybridization GISH)
Metoda stosowana w cytogenetyce roślin. Jako sondy używa się w niej całego genomowego DNA, którym znakuje się chromosomy mitotycznych lub mejotycznych mieszańców. Pozwala m.in. na identyfikację gatunków rodzicielskich oraz ustalenie wzajemnego pokrewieństwa między taksonami.
Genomowa hybrydyzacja porównawcza (ang. comparative genomie hybridization CGH)
To metoda stosowana w diagnostycznej cytogenetyce molekularnej do identyfikacji niektórych typów nowotworów. Pozwala na identyfikację zmian (delecji, duplikacji i amplifikacji) w chromosomach. Polega na podwójnej hybrydyzacji z sondami pochodzącymi ze zdrowych i nowotworowych komórek.
Synteza in situ przy udziale startera (ang. primed in situ labelling PRINS)
Nieoznakowaną sondę łączy się z wybranym odcinkiem kwasu nukleinowego. Pełni ona funkcję startera dla polimerazy, która do budowy nowego fragmentu wykorzystuje znakowane nukleotydy. Wykrywa się je za pomocą mikroskopu fluorescencyjnego.
Literatura:
• Jerzy Bal „Biologia molekularna w medycynie. Elementy genetyki klinicznej”; Wydawnictwo Naukowe PWN; Warszawa 2001;
• Anna Raszka, Aleksandra Ziembińska, Anna Wiechetek „Metody i techniki biologii molekularnej w biotechnologii środowiskowej”; Środowisko, Czasopismo Techniczne; Wydawnictwo Politechniki Krakowskiej; Zeszyt 2, rok 2009;
• Janusz Piechota „Analiza typu Northern blot”; http://metlab.pl/; 2009;
• materiały z ćwiczeń do przedmiotu inżynieria chromosomowa (Uniwersytet Szczeciński). )

