Białka są to wielkocząsteczkowe polimery odgrywające kluczową rolę we wszystkich procesach biologicznych. Ich podstawową jednostką strukturalną są aminokwasy zbudowane z grupy aminowej, karboksylowej, atomu wodoru i łańcucha bocznego – R. Tetraedryczne ułożenie podstawników wokół węgla α nadaje cząsteczce aminokwasu charakter związku optycznie czynnego, jednak wyłącznie izomery lewoskrętne, czyli L-aminokwasy mogą wchodzić w skład białek. Ich rodzaj i wzajemne powiązanie decydują o właściwościach i funkcji budowanej cząsteczki.
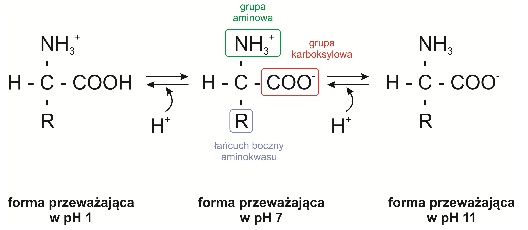
Rys. 1. Budowa i stopień jonizacji aminokwasu w zależności o d pH roztworu
W białkach występuje powszechnie dwadzieścia rodzajów aminokwasów, które różnią się między sobą kształtem, wielkością, ładunkiem elektrycznym i reaktywnością chemiczną łańcuchów bocznych. Najprostszym aminokwasem jest glicyna, której łańcuch boczny stanowi pojedynczy atom wodoru.

Rys. 2. Aminokwasy budujące białka
Zespolenie grupy karboksylowej jednego aminokwasu z grupą aminową drugiego aminokwasu nazywa się wiązaniem peptydowym. Podczas jego powstawania uwalniana jest jedna cząsteczka wody.
Łańcuch aminokwasowy składa się z części głównej (szkieletu) oraz łańcuchów bocznych. Oba jego końce są reaktywne, przy czym grupa aminowa wyznacza jego początek, a reszta karboksylowa koniec. Struktury złożone z kilku – kilkunastu monomerów nazywa się oligopeptydami, natomiast kilkadziesiąt reszt aminokwasowych tworzy strukturę polipeptydu. Duże, złożone białka mogą zawierać kilka takich łańcuchów oraz dodatkowe elementy niebiałkowe, takie jak reszty cukrowe, lipidowe, czy jony metali.
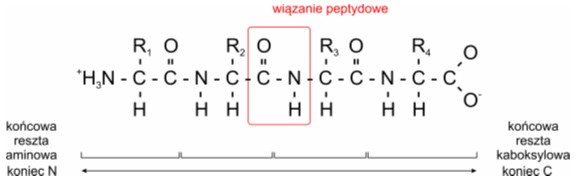
Rys. 3. Tetrapeptyd
Wzajemne oddziaływanie reszt aminokwasowych powoduje powstawanie bardziej skomplikowanych struktur, których poziom organizacji określa się mianem rzędowości. Proces fałdowania się białek (ang. folding) może zachodzić spontanicznie lub przy udziale chaperonów. Przestrzenne ułożenie łańcucha polipeptydowego (konformacja), wpływa na właściwości cząsteczki i pełnione przez nią funkcje. Zmiany w strukturze prowadzą do utraty aktywności biologicznej białka i nazywane są deformacją.
Struktura pierwszorzędowa to sekwencja aminokwasów w łańcuchu polipeptydowym. Wyznaczana jest ona przez kolejność nukleotydów budujących cząsteczkę DNA. Wiele białek po zsyntetyzowaniu ulega jednak dalszej obróbce.
Na strukturę drugorzędowa wpływają głównie właściwości płaskich wiązań peptydowych. Umożliwiają one cząsteczce obrót jedynie w miejscu wiązania C-Cα (kąt psi ψ) i Cα-. N (kąt torsyjny – fi φ). Na podstawie wartości tych kątów można określić konformację łańcucha głównego. Grupy boczne sąsiednich aminokwasów wzajemnie ograniczają swoje zdolności rotacyjne. Istnieją dwa typy regularnych układów drugorzędowych:
• α- helisa – ma charakter dipolowy, tzn. niepolarny rdzeń otaczają polarne grupy boczne ułożeniu heliakalnie po zewnętrznej stronie. W białkach występują głównie helisy prawoskrętne. Struktura ta stabilizowana jest wiązaniami wodorowymi powstającymi między grupą CO aminokwasu, a grupą NH aminokwasu oddalonego o cztery reszty aminokwasowe. Na jeden obrót helisy przypada 3,6 reszt aminokwasowych, natomiast skok helisy wynosi 0,54 nm. Każda reszta aminokwasowa jest przesunięta w stosunku do sąsiedniej o 0,15 nm wzdłuż osi helisy i obrócona o 100° wokół osi;
• β-harmonijka (β- kartka) – przyjmuje rozciągnięty kształt. Odległość pomiędzy sąsiadującymi aminokwasami wynosi 0,35 nm. Struktura ta stabilizowana jest wiązaniami wodorowymi tworzącymi się pomiędzy grupami CO i NH aminokwasów leżących w jednej płaszczyźnie. Może być ona utworzona przez kilka łańcuchów polipeptydowych ułożonych w jednym kierunku (równoległa β-harmonijka) lub w kierunku przeciwnym (antyrównoległa β-harmonijka).
Z uwagi na właściwości hydrofobowe łańcuchów bocznych, struktury α-helisy i β- harmonijki mogą oddziaływać między sobą tworząc złożone motywy. Pełnią one kluczową rolę podczas fałdowania się białka.
• „szpilka do włosów” (ang. harpin loop) składa się z antyrównoległej struktury β podtrzymywanej przez pojedynczy łańcuch polipeptydowy. Odwrócenie łańcucha tworzy się dzięki wiązaniom wodorowym pomiędzy grupą CO reszty n aminokwasu, a grupą NH reszty n+3 aminokwasu;
• „klucz grecki” – rozbudowany motyw „szpilki do włosów”, w którym jeden łańcuch polipeptydowy tworzy cztery antyrównoległe struktury β-harmonijki;
• „heliks-pętla-heliks” (ang. helix-turn-helix) ten motyw α-helisy występuje głównie w białkach wiążących DNA;
• „suwaki leucytowe” – składają się z dwóch splecionych ze sobą i bogatych w leucynę α-helis. Dzięki zasadowemu charakterowi struktura ta ma duże powinowactwo do DNA;
• βαβ to rodzaj motywu mieszanego, w którym α-helisa usytuowana jest pomiędzy dwoma równolegle ułożonymi łańcuchami β-harmonijki, w taki sposób, że hydrofobowe strony obu łańcuchów kontaktują się ze sobą.
Białka mogą być zbudowane z kilku, niezależnie pofałdowanych łańcuchów tworzących struktury zwane domenami, np. domena globinowa zbudowana z czterech struktur α-helikalnych tworzących motyw „heliks-pętla-heliks”. Stanowią one często części funkcjonalne białek, np. centra katalityczne enzymów.
Struktura trzeciorzędowa powstaje się w wyniku tworzenia się wiązań (innych niż wodorowe) pomiędzy aminokwasami – np. mostków solnych lub mostków dwusiarczkowych. Ważną rolę odgrywa także oddziaływanie reszt aminokwasowych z rozpuszczalnikiem. Reszty hydrofobowe rozpuszczalnych w wodzie białek koncentrują się we wnętrzu cząsteczki, natomiast niosące ładunek reszty polarne wysuwają się na zewnątrz i ulegają hydratacji.
Struktura czwartorzędowa charakteryzuje białka oligomeryczne, czyli złożone z kilku podjednostek. Ona również stabilizowana jest za pomocą wzajemnych oddziaływań między resztami aminokwasowymi oraz wpływom rozpuszczalnika.
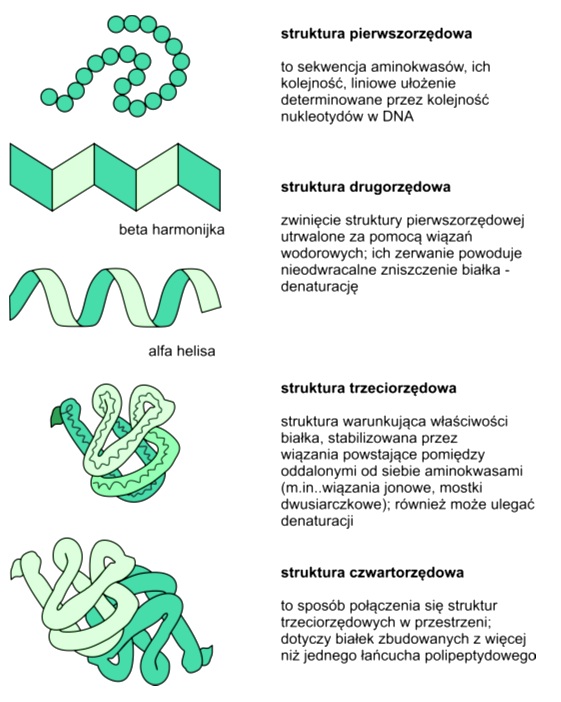
Rys. 4. Rzędowość struktury białek
Autor: Anna Kurcek
Literatura:
• Lubert Stryer „Biochemia”; Wydawnictwo Naukowe PWN; Warszawa 2003;
• Robert K. Murray, Daryl K. Granner, Peter A. Mayes, Victor W. Rodwell “Biochemia Harpera Wydanie III”; Wydawnictwo Lekarskie PZWL; Warszawa 1995;
• Ewa Pyłka-Gutowska „Biologia, Vademecum Maturzysty”; Wydawnictwo „OŚWIATA”, Warszawa 2002.

