PRZEDRUK, oryginał dostępny pod adresem www
Fragmenty skryptu: Materiały do ćwiczeń laboratoryjnych z chemii organicznej dla studentów farmacji: wstęp
Autor skryptu: prof. UJ dr hab. Marek Cegła, dr Barbara Drożdż
Uniwersytet Jagielloński (www)
Wydział Farmaceutyczny Collegium Medicum (www)
Katedra Chemii Organicznej (www)
Kierownik: Prof. UJ, dr hab. Marek Cegła
Adres:
ul. Medyczna 9
30-688 Kraków
Kontakt: tel. 012 620 55 00
Reakcje chemiczne prowadzi się najczęściej w szklanych naczyniach wykonanych z wysokiej jakości szkła borokrzemianowego, odpornego na działanie większości substancji chemicznych (z wyjątkiem HF). Szkło takie w temperaturze pokojowej odporne jest także na działanie zasad, ale w wyższych temperaturach i po dłuższym czasie może ulegać trawieniu. Niektóre reakcje prowadzi się w naczyniach kwarcowych lub z tworzyw sztucznych takich jak polietylen, polipropylen czy teflon. Ten ostatni jest niezwykle odporny chemicznie i trwały do temperatury ok. 200 oC, ale niestety bardzo drogi. Czasami korzysta się z naczyń porcelanowych (lejki, tygle, moździerze).
Zlewki, cylindry, pipety
Powszechnie stosowane w laboratoriach są zlewki różnego kształtu i pojemności, służące do sporządzania roztworów, przygotowywania reagentów czy czasami nawet prowadzenia prostych reakcji. Należy pamiętać jednak, że nie jest to szkło miarowe i zaznaczone na nich podziałki mają jedynie charakter orientacyjny i w żadnym razie nie mogą być podstawą obliczeń stechiometrycznych.
Do dokładnego odmierzania objętości cieczy służą cylindry miarowe (menzurki) i pipety.

Zlewka

Cylindry miarowe
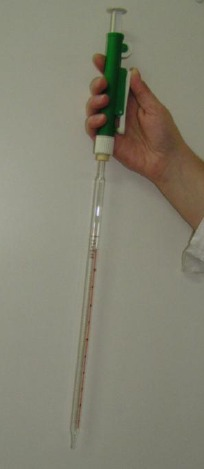
Pipeta
Kolby
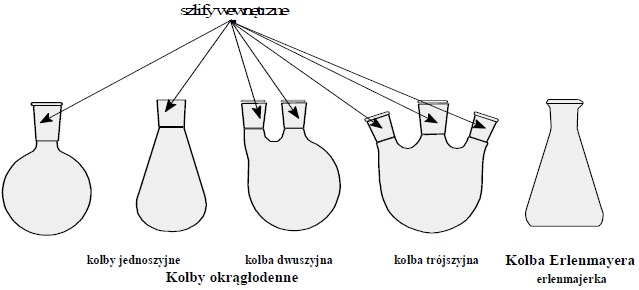
Do najczęściej używanych w laboratorium naczyń szklanych służących do prowadzenia procesów chemicznych należą różnego typu kolby. Wśród nich do najczęściej używanych zaliczamy kolby:
– okrągłodenne (czasem o kształcie gruszkowatym, z szyjkami o różnej długości i średnicy)
– kolby wieloszyjne, w których montowane są mieszadła, wkraplacze, chłodnice, termometry i inne potrzebne do przeprowadzenia danej reakcji urządzenia.
– kolby płaskodenne
– kolby stożkowe (tzw. erlenmajerki – nazwa pochodzi od nazwiska niemieckiego chemika E. Erlenmeyera
Większość obecnie produkowanego szkła laboratoryjnego zaopatrzona jest w znormalizowane szlify szklane, tzn. jeden z łączonych elementów ma zeszlifowaną i zmatowiona powierzchnię zewnętrzną (tzw. szlif zewnętrzny) a drugi wewnętrzną (tzw. szlif wewnętrzny). Elementy te mają ściśle określoną geometrię, są produkowane w standardowych wielkościach i doskonale pasują do siebie, zapewniając szczelność połączenia. Pozwala to szybko budować wiele typowych zestawów z kilku podstawowych elementów.

Należy pamiętać, że przy pracy z substancjami silnie zasadowymi powierzchnie szlifów chroni się specjalnymi smarami. Trzeba też zwrócić uwagę, aby pomiędzy powierzchnie szlifów nie dostawały się reagujące substancje, gdyż bardzo często, szczególnie w podwyższonej temperaturze, powoduje to trwałe zespolenie elementów zestawu. Dobierając poszczególne elementy zestawu do przeprowadzenia planowanej reakcji chemicznej, należy zwrócić uwagę na dostosowanie wielkości używanych naczyń laboratoryjnych do skali eksperymentu, tak aby z jednej strony po dodaniu wszystkich reagentów kolba reakcyjna była wypełniona nie więcej niż w 2/3 swojej objętości, a z drugiej, aby nie stosować np. litrowej kolby do ogrzewania 10 cm3 roztworu. Stosowanie szkła o zbyt dużej objętości prowadzi do strat ilościowych i świadczy o braku umiejętności laboratoryjnych.
Chłodnice
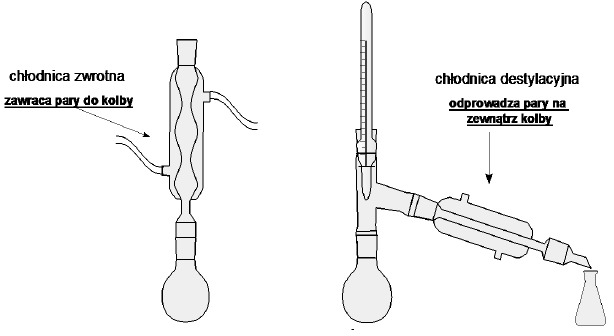
Ogrzewanie ciekłych reagentów w trakcie prowadzenia reakcji chemicznych wymaga schładzania powstających par i zawracania ich do naczynia reakcyjnego lub odprowadzania schłodzonych par na zewnątrz. W pierwszym wypadku mówimy o tzw. chłodnicach zwrotnych w drugim o chłodnicach destylacyjnych. Chłodnice te zaopatrzone są zazwyczaj w połączenia szlifowe i montuje się je w szyjach kolb.
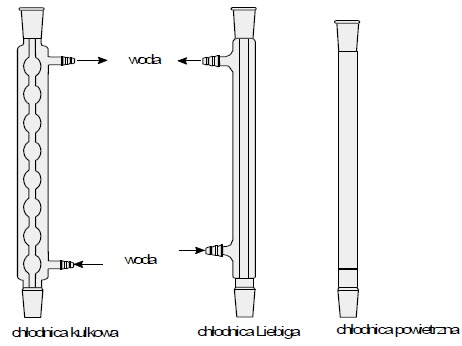
Rodzaj chłodnicy dobiera się w zależności od temperatury wrzenia cieczy, której pary chcemy schładzać. Pary cieczy wrzących do 100°C schładza się najczęściej chłodnicami Liebiga, czyli szklanymi rurami obudowanymi płaszczem wodnym, przez który przeciwprądowo przepływa woda wodociągowa. Pary cieczy wrzących w temperaturach od 100oC do 150oC chłodzi się za pomocą chłodnic Liebiga z zamkniętym przepływem wody a do par o wyższych temperaturach używa się chłodnic powietrznych, w których rolę płaszcza chłodzącego spełnia otaczające powietrze.
Chłodnice zwrotne
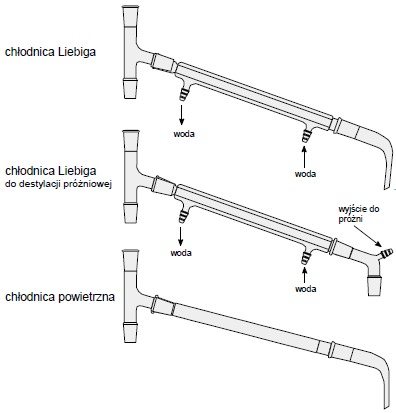
Chłodnice destylacyjne
Rozdzielacze, wkraplacze
Rozdział niemieszających się ze sobą cieczy przeprowadza się za pomocą rozdzielaczy o różnych kształtach i pojemności. Korki i krany tych naczyń mogą być wykonane z doszlifowanego szkła lub teflonu. Takie same lub podobne naczynia służą jako wkraplacze, które umieszczone np. w szyjach kolb, służą do dozowania ciekłych reagentów do mieszaniny reakcyjnej. Ich nóżki wyposażone są wtedy zazwyczaj w szlif zewnętrzny.
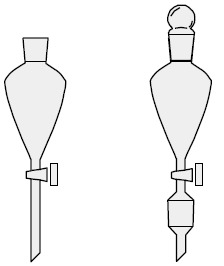
Rozdzielacz (lub wkraplacz)

Sposób montowania
Mycie i suszenie szkła laboratoryjnego
Szklane naczynia przeznaczone do prac laboratoryjnych muszą być czyste i najczęściej dokładnie wysuszone.
Dobór rozpuszczalnika do mycia powinien być dostosowany do rodzaju zanieczyszczeń i wymagań prowadzonego procesu. Najczęściej mycie rozpoczyna się w wodzie z użyciem popularnych detergentów. Należy używać szczotek tak aby nie dotykać gołą ręką zanieczyszczonych powierzchni. Osady nierozpuszczalne w wodzie można usuwać za pomocą niewielkich ilości acetonu.
O tym czy szkło musi być suche decyduje rodzaj prowadzonego procesu, a także postać dodawanych odczynników. Jeżeli używa się roztworów wodnych to oczywiście można używać wilgotnego szkła. Szkło można suszyć w suszarkach, pamiętając aby nie umieszczać w nich naczyń zawierających elementy plastikowe lub gumowe, które mogą ulec zniszczeniu. Innym sposobem suszenia jest przepuszczanie przez nie strumienia gorącego powietrza (np. za pomocą suszarki do włosów).Przepłukanie szkła acetonem znacznie przyspiesza proces suszenia.

